 Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Aufgabensammlung für das Fach Chemie in der Schule
Elektrochemie: Redoxreaktionen sorgen für Spannung
Nernst'sche Gleichung - Faraday`sche Gesetze
1. Folgende Konzentrationszellen werden untersucht:
Ag/Ag+//Ag/Ag+ und Pb/Pb2+//Pb/Pb2+.
a) Beschreibe die Vorgänge, die zur Ausbildung des elektrochemischen Potentials führen, indem du ein Element zeichnest, die Zeichnung beschriftest und dann die Vorgänge im atomaren Bereich erklärst und begründest.
b) Beschreibe die Beziehung, die sich zunehmender Verdünnung für das elektrochemische Potential formulieren läßt und begründe diese Beziehung aus den Überlegungen in a)
2. Ein Zinkstab taucht in eine Zinksalzlösung, die im unteren Teil konzentrierter ist als im oberen Teil Teil.
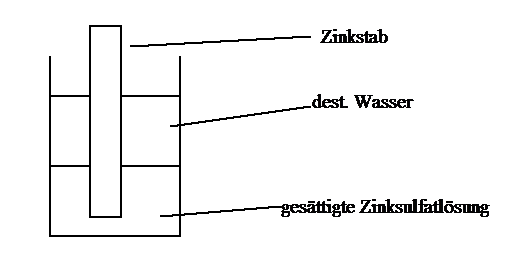
Nach einigen Stunden beobachtet man, daß sich am unteren Teil des Zinkstabes Zinkkristalle abscheiden.
Beschreibe und analysiere die Versuchsergebnisse in Hinblick auf die Gesetzmäßigkeiten der Elektrochemie.
3.Wie lauten die Faraday'schen Gesetze?
4. Wie lange muß eine Strom von 1000 A fließen, wenn 1 t Kupfer aus Kupfersulfatlösung abgeschieden werden soll?
6. Bei einer Elektrolyse werden aus einer Zinksulfatlösung 10 g Zink abgeschieden.
Wieviel g Kupfer bilden sich unter gleichen Bedingungen?
7. Welche Formeln haben folgende Stoffe? Wie dissoziieren sie (wenn löslich) in Wasser?
Silbernitrat Silbersulfat Zinksulfat Natriumchlorid Salpetersäure Essigsäure Salzsäure Schwefelsäure Bleichlorid Silberchlorid Aluminiumchlorid Wasserstoffperoxid Bromwasserstoff Schwefelswasserstoff Kupfersulfat Kupfersulfit Kupfersulfid Schweflige Säure Natronlauge Calciumhydroxid Alumniumhydroxid Alumniumoxid Kupferoxid Bleinitrat Zinknitrat Lithiumiodid Bleiiodid Kohlensäure Natriumcarbonat Kupferacetat Bleiacetat Silberbromid
Matthias Rinschen (C) 2006 - 2024, Mail: deinchemielehrer [at] gmx [dot] de, Impressum und Datenschutzerklärung