 Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Aufgabensammlung für das Fach Chemie in der Schule
Seiten für Schüler
Zur Abiturvorbereitung
Fragen zur allgem. ChemieFragen zum MWG Fragen zur ElektrochemieFragen zu Säuren und BasenFragen zur Org. ChemieFragen zu FarbstoffenChemie kurz und Knapp
Bohr'sches Atomodell oder Orbitalmodell - Welches Atommodell benötigt man wofür?Zwischenmolekulare Kräfte - Bindungsarten - AggregatzuständeBindungsarten - Ionenbindung - kovalente Bindung - polarisierte kovalente BindungBindungen in der organischen ChemieMesomerieWarum sind alle Metalle Reduktionsmittel?Wie erkenne ich, welche Vorgänge bei einer Elektrolyse ablaufen? Was ist eigentlich der Diffusionsstrom? Welche Auswirkung hat die Überspannung?
Organische Chemie:
Qualitative Elementaranalyse
Man unterscheidet zwischen der qualitativen und der quantitativen Elementaranalyse. Bei der ersten untersucht man, welche Elemente eine Verbindung aufbauen, bei der zweiten untersucht man, in welchen Massenverhältnis die aufbauenden Elemente stehen, um daraus die Verhältnisformel (Zahlenverhältnis der einzelnen Atome zueinander) der Verbindung zu bestimmen. Zum Schluß führt man noch eine Molekülmassenbestimmung durch, sodaß man die genaue Verhältnisformel angeben kann.
Qualitative Elementaranalyse: Welche Atome sind Bestandteil einer Verbindung?
Entwickelt wurde dieses Verfahren unter anderem von Justus von Liebig (Gießen) (1803 – 1873).
Dabei verbrennt man die organische Verbindung, läßt sie also mit Sauerstoff reagieren. Alle Elemente der Verbindung, die mit Sauerstoff reagieren, bilden dabei die entsprechenden Oxide. Diese weist man dann durch die bekannten Reaktionen nach:
Kohlenstoff in der Verbindung reagiert mit Sauerstoff zu Kohlenstoffdioxid-
Kohlenstoffdioxid ergibt mit Calciumhydroxidlösung einen weißen Niederschlag.
(Die Lösung wird trüb)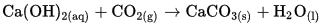
Wasserstoff in der Verbindung reagiert mit Sauerstoff zu Wasser.
Dieses zeigt sich in kleinen Tröpfchen an den kühlen Stellen des Reaktionsgefäßes. Weißes Kupfersulfat CuSO4 nimmt dieses Wasser als Kristallwasser auf. Das Kristallwasser ist in die Struktur des Kristalles eingebaut. CuSO4 nimmt 5 H2O pro Mol auf. Es ist dann blau.
Sauerstoff kann man natürlich nicht durch die Verbrennung nachweisen. Man benutzt dazu ein starkes Reduktionsmittel, also einen Stoff. der sehr gut Sauerstoff aufnimmt. In diesem Fall gelingt das mit Magnesium. Dieses entreißt der organischen Verbindung bei hoher Temperatur den Sauerstoff und wird zu MgO , Magnesiumoxid, welches ein weißes Pulver ist, alkalisch reagiert und deshalb in Wasser gegebenes Phenolphthalein rot färbt.
Matthias Rinschen (C) 2006 - 2024, Mail: deinchemielehrer [at] gmx [dot] de, Impressum und Datenschutzerklärung