 Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Aufgabensammlung für das Fach Chemie in der Schule
Aufgaben mit Lösungen: Organische Chemie
ElektrochemieOrganische Chemie
Übersicht org. Chemie Eigenschaften und Reaktionen des PhenolsEigenschaften und Reaktionen des Phenols
Eigenschaften und Reaktionen des AnilinsDarstellung und Weiterverarbeitung eines Kunststoffes
Eigenschaften und Reaktionen des Phenols
Bei den demonstrierten Experimenten werden außer Phenol noch Wasser, Salzsäure und Natronlauge sowie halbkonzentrierte Salpetersäure und ein Gerät zur Messung des pH-Wertes verwendet.
Formel des Phenols: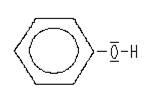
Aufgaben
a)Beschreiben Sie die Versuche und Ihre Beobachtungen.
b) Erörtern und begründen Sie die Eigenschaften des Phenols gegenüber Wasser, Säuren und Laugen.
c)Analysieren Sie Ihre Beobachtungen bei der Reaktion von Phenol mit halbkonzentrierter Salpetersäure. Erklären Sie die abgelaufene Reaktion, formulieren Sie deren Reaktionsmechanismus und stellen Sie die Reaktion vergleichend der analogen Reaktion des Benzols gegenüber.
d) Definieren Sie ausgehend vom Massenwirkungsgesetz den Ks-Wert und beurteilen Sie die Acidität des Reaktionsproduktes der Reaktion von Phenol mit Salpetersäure im Vergleich zu der Acidität des Phenols selbst. Begründen Sie Ihre Darlegungen.
Lösung
a) Experimente:
Phenol ist in Wasser mäßig löslich, seine Reaktion ist sauer.
In Natronlauge ist es gut löslich, bei Zugabe von Salzsäure fällt es wieder aus.
Sofortige, heftige Reaktion mit halbkonzentrierter Salpetersäure
b)Lösungsverhalten
geringe Löslichkeit in Wasser auf Grund des großen, unpolaren Restes, dabei aber leicht saure Reaktion: Formulierung der Protolysenreaktion, Begründung durch Mesomerieeffekte der OH-Gruppe, Löslichkeitserhöhung in alkalischen Lösungen auf Grund der Salzbildung, Prinzip von Le Chatelier: Verschiebung des Gleichgewichts der Reaktion von Phenol mit Wasser durch Zugabe von Hydroxidionen, Umkehrung der Salzbildungreaktion durch Zugabe einer starken Säure
c)Heftige und schnelle Reaktion von Phenol mit Salpetersäure auf Grund des + M -Effektes der - OH Gruppe. Begründung der erhöhten Reaktivität im Vergleich zu Benzol durch entsprechende mesomere Grenzstrukturen. Formulierung des Mechanismusses der Nitrierung, dabei Entstehung des elektrophilen Agens durch Autoprotonierung der Salpetersäure im Gegensatz zu der Reaktion von Benzol, bei der konz. Schwefelsäure zugefügt wird,
Erläuterung und Begründung des Ortes der Nitrierung durch mesomere Grenzstrukturen
d) Die Acidität des Nitrophenols ist höher als die des Phenols, da durch den - M - Effekt der Nitrogruppe die Abspaltung des Protons an der OH-Gruppe erleichtert ist: Formulierung der Protolysenreaktion, Definition der Säurestärke durch Reaktionsschemata und MWG, Beleg der erhöhten Stabilität des Nitrophenolations durch mesomere Grenzstrukturen (chinoide Strukturen)
Matthias Rinschen (C) 2006 - 2024, Mail: deinchemielehrer [at] gmx [dot] de, Impressum und Datenschutzerklärung